威尔康奈尔医学院的研究人员开发了一种计算方法,可以前所未有地详细绘制人体组织的结构图。他们的方法有望加速对器官规模细胞相互作用的研究,并可以为多种疾病提供强大的新诊断策略。
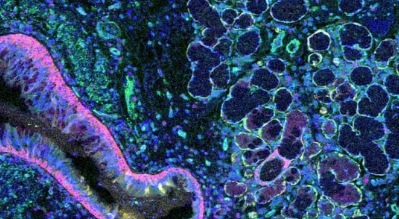
该方法发表在NatureMethods上,源于科学家对经典显微镜和现代单细胞分子分析之间的差距感到沮丧。
“在显微镜下观察组织,你会看到一堆在空间上聚集在一起的细胞——你几乎可以立即在图像中看到这种组织,”主要作者、威尔康奈尔医学院生理学和生物物理学研究生JunbumKim说。“现在,细胞生物学家已经能够非常详细地检查单个细胞,甚至每个细胞表达的基因,因此他们专注于细胞而不是组织结构。”
然而,“对于研究人员来说,了解更多关于组织结构的细节是至关重要的;组织内细胞之间关系的根本变化驱动着健康和患病的器官功能,”资深作者OlivierElemento说,他是英格兰德精密医学研究所所长,威尔康奈尔大学生理学和生物物理学以及计算生物医学计算基因组学教授药物。
然而,手动将单细胞数据与组织结构图相结合既缓慢又乏味。机器学习算法已经显示出一些自动化过程的潜力,但它们受到用于训练它们的数据的限制。为了解决这个问题,Kim和他的同事开发了一种无监督计算策略,结合单细胞基因表达谱和细胞位置来定义组织的结构区域。
共同资深作者AndreRendeiro是研究期间威尔康奈尔医学院的博士后研究员,目前是奥地利维也纳奥地利科学院分子医学研究中心的首席研究员,他将新方法与绘制城市地图进行了比较纽约:“解决这个问题的一种方法是去每个十字路口,数一数每种建筑物:它是住宅的,是商业的……是商店还是餐馆?”将所有这些数据放入一个矩阵,将建筑物的位置放入另一个矩阵,可以揭示两个矩阵组合时的模式。
“从本质上讲,我们可以开始根据住宅和商业建筑的数量,对不同社区的位置和边界位置做出一般性声明——就像任何人穿过上东区、中城或市中心时所做的那样根据他们的观察,”Rendeiro说。
研究人员使用这种新方法生成了几种组织的详细图谱,识别和量化了显微解剖学的新方面——细胞相互作用时小规模出现的模式,并决定了组织的最终功能。他们与北卡罗来纳大学教堂山分校研究肺部疾病的同事合作,还证明了他们的技术可以在组织中的不同疾病状态之间做出细微的区分。
虽然癌症和其他慢性疾病通常会导致组织结构发生重大变化,但详细的显微解剖学也有助于诊断和治疗更严重的疾病。Rendeiro以严重的COVID-19为例,其中“有很多免疫细胞移动到附近,肺组织确实发生了巨大变化。”该团队现在正在将其新技术应用于广泛的组织,以了解组织组织的变化如何影响其在健康状态下的功能和疾病中的功能障碍。
